1
/
von
12
PayPal, credit cards. Download editable-PDF & invoice in 1 second!
YY 0844-2011 Englisch PDF (YY0844-2011)
YY 0844-2011 Englisch PDF (YY0844-2011)
Normaler Preis
$150.00 USD
Normaler Preis
Verkaufspreis
$150.00 USD
Grundpreis
/
pro
Versand wird beim Checkout berechnet
Verfügbarkeit für Abholungen konnte nicht geladen werden
Lieferung: 3 Sekunden. True-PDF + Rechnung herunterladen.
Erhalten Sie in 1 Minute ein ANGEBOT: Klicken Sie auf YY 0844-2011
Historische Versionen: YY 0844-2011
Vorschau von True-PDF (Neu laden/Scrollen, wenn leer)
YY 0844-2011: Lasertherapiegerät. Behandlungsgerät mit gepulstem Kohlendioxidlaser
JJ 0844-2011
JJ
PHARMAZEUTISCHER INDUSTRIESTANDARD
DER VOLKSREPUBLIK CHINA
ICS 11.040.60
C 41
Lasertherapiegeräte –
Gepulstes Kohlendioxid-Laser-Behandlungsinstrument
激光治疗设备
AUSGESTELLT AM 31. DEZEMBER 2011
IMPLEMENTIERT AM 01. JUNI 2013
Herausgegeben von der chinesischen Arzneimittel- und Lebensmittelbehörde
Inhaltsverzeichnis
Vorwort ... 3
1 Geltungsbereich ... 4
2 Normative Verweisungen ... 4
3 Begriffe und Definitionen ... 5
4 Produktzusammensetzung und Grundparameter ... 6
5 Anforderungen ... 9
6 Prüfmethoden ... 14
7 Inspektionsregeln ... 19
8 Kennzeichnung, Etikett und Bedienungsanleitung ... 20
9 Verpackung, Transport und Lagerung ... 22
Vorwort
Dieser Standard wurde entsprechend den in GB/T 1.1.2009 festgelegten Regeln erstellt.
Diese Norm implementiert GB 9706.1-2007 „Medizinische elektrische Geräte - Teil
1. Allgemeine Anforderungen an die Sicherheit“, GB 9706.20-2000 „Medizinische elektrische
Geräte - Teil 2. Besondere Anforderungen an die Sicherheit von Diagnose- und
therapeutische Lasergeräte“ UND GB 7247.1-2001 „Sicherheit von Laserprodukten –
Teil 1. Geräteklassifizierung, Anforderungen und Benutzerhandbuch“.
Bitte beachten Sie, dass einige der Inhalte dieses Dokuments sich auf
Patente. Der Herausgeber dieses Dokuments ist nicht verantwortlich für die Identifizierung solcher
Patente.
Dieser Standard wurde von der China Food and Drug Administration vorgeschlagen.
Dieser Standard unterliegt der Zuständigkeit der National Medical Optics und
Technischer Ausschuss für Instrumentenstandardisierung (SAC/TC 103/SC 1).
Dieser Standard wurde von der China Food and Drug Administration Hangzhou erstellt
Zentrum für Qualitätsüberwachung und Inspektion von Medizinprodukten, Zhejiang Medical
Device Testing Institute und Chongqing Jingyu Laser Technology Co., Ltd.
Die Hauptverfasser dieser Norm. Han Jiancheng, Zhou Zhikang, Du Kun, Ye
Yueshun, Kong Peng.
Lasertherapiegeräte –
Gepulstes Kohlendioxid-Laser-Behandlungsinstrument
1 Geltungsbereich
Diese Norm legt die grundlegenden Parameter und die Zusammensetzung des Produkts fest.
technische Anforderungen, Prüfmethoden, Kennzeichnung Etiketten und Verpackung von gepulsten
Kohlendioxid-Laserbehandlungsgerät. Diese Norm bietet technische
Spezifikationen für Hersteller von gepulsten Kohlendioxid-Laserbehandlungen
Instrument zur Entwicklung von Produktnormen für Medizinprodukte.
Diese Norm gilt für den gepulsten Betriebsabschnitt der gepulsten Kohlenstoff
Kohlendioxid-Laserbehandlungsgerät mit nur gepulstem Betriebsmodus
UND das gepulste Kohlendioxid-Laser-Behandlungsinstrument, das sowohl die
Dauerwellenbetrieb und gepulster Betrieb (im Folgenden
einfach als Behandlungsinstrument bezeichnet) eines Kohlendioxidlasers
therapeutische Geräte, die sowohl a. Der Begriff „Puls“ in dieser Norm hat
die Pulsdauer (Pulsbreite) weniger als 0,25 s. Das Behandlungsinstrument ist,
über den Pulslaser mit einer Wellenlänge von 10,6 μm, der Verdampfung durchführt,
Karbonisierung, Koagulation und Bestrahlung des menschlichen Gewebes, um
den Behandlungszweck zu erreichen.
Was das gepulste Kohlendioxid-Laser-Behandlungsinstrument betrifft, das sowohl die
Dauerwellenbetrieb und gepulster Betrieb, der Dauerwellenbetrieb
Der Wellenbetrieb muss GB 11748 entsprechen, und der gepulste Betrieb
Der Modus muss diesem Standard entsprechen.
2 Normative Verweisungen
Die folgenden Dokumente sind für die Anwendung dieses Dokuments erforderlich.
die datierten Dokumente, es gelten nur die Versionen mit den angegebenen Daten
zu diesem Dokument; für die undatierten Dokumente gilt nur die neueste Version (einschließlich
alle Änderungen) sind auf diesen Standard anwendbar.
GB/T 191 Verpackung - Bildliche Kennzeichnung für den Umgang mit Waren
GB 7247.1 Sicherheit von Laserprodukten - Teil 1. Geräteklassifizierung,
Anforderungen und Benutzerhandbuch
GB 9706.1 Medizinische elektrische Geräte - Teil 1. Allgemeine Anforderungen an
Sicherheit
GB 9706.20 Medizinische elektrische Geräte - Teil 2. Besondere Anforderungen
für die Sicherheit diagnostischer und therapeutischer Lasergeräte
GB/T 14710 Umweltanforderungen und Prüfverfahren für medizinische
Elektrische Ausrüstung
GB/T 17736 Prüfverfahren für die wichtigsten Parameter von Laserschutzbrillen
YY 91057 Allgemeine Spezifikation für medizinische Fußschalter
ISO 11146 Laser und laserbezogene Einrichtungen - Prüfverfahren für Laserstrahlen
Breiten, Divergenzwinkel und Strahlausbreitungsverhältnisse
3 Begriffe und Definitionen
Die Begriffe und Definitionen wie in GB 7247.1 definiert UND die folgenden gelten für
dieses Dokument.
3.1
50%-Pulsdauer
τ50
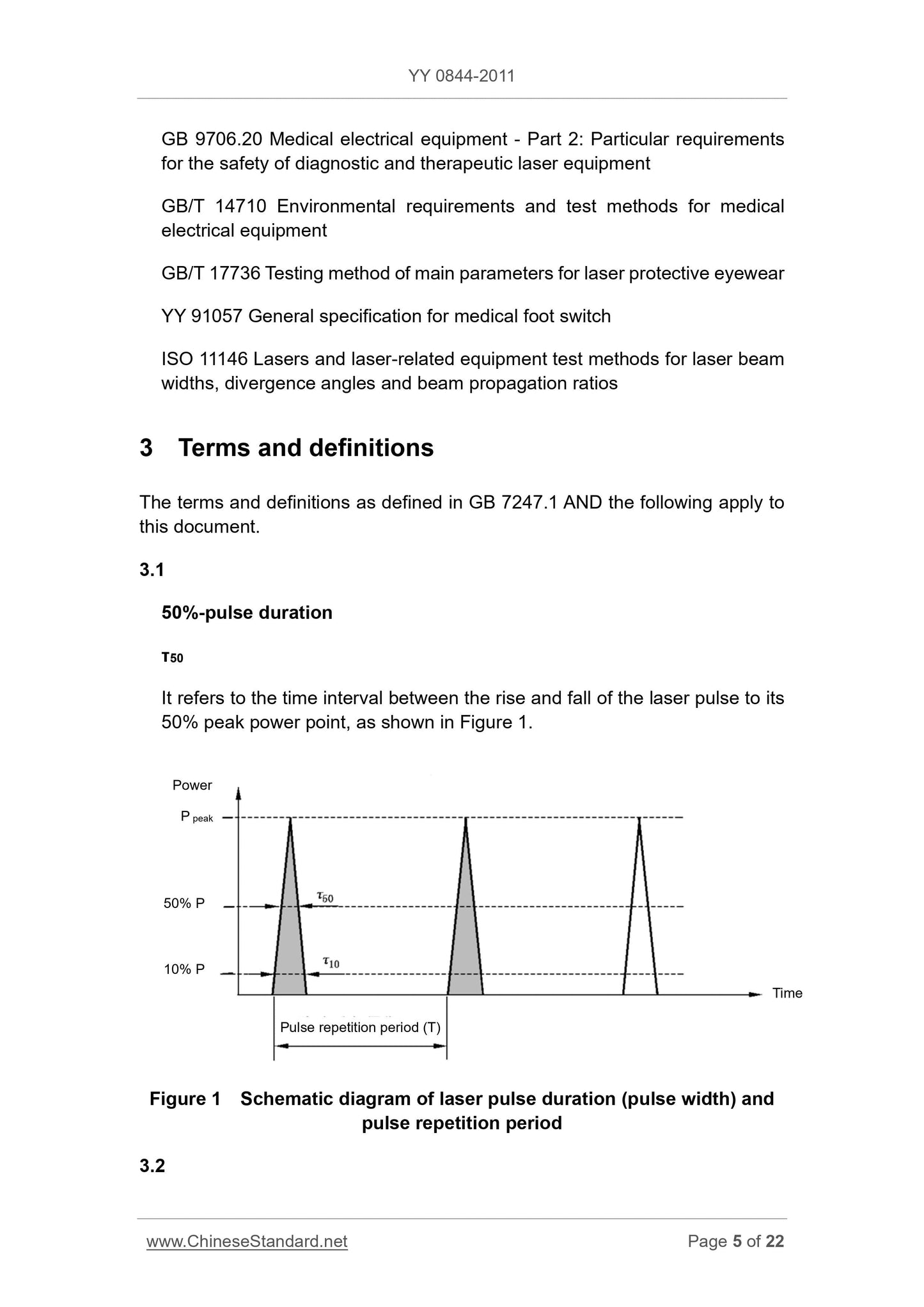
Es bezeichnet die Zeitspanne zwischen dem Anstieg und Abfall des Laserpulses bis zu seiner
50 % Spitzenleistungspunkt, wie in Abbildung 1 dargestellt.
Abbildung 1 Schematische Darstellung der Laserpulsdauer (Pulsbreite) und
Pulswiederholperiode
3.2
Zeit
Leistung
P-Spitze
50 % P
10 % P
Pulswiederholperiode (T)
10%-Pulsdauer
τ10
Es bezeichnet die Zeitspanne zwischen dem Anstieg und Abfall des Laserpulses bis zu seiner
10 % Spitzenleistungspunkt, wie in Abbildung 1 dargestellt.
3.3
50%-Pulsleistung
P50
P50 ist das Verhältnis von Pulsenergie Q zu 50%-Pulsdauer (50% Pulsbreite)
τ50, wie in Gleichung (1) gezeigt.
3.4
10%-Pulsleistung
Platz 10
P10 ist das Verhältnis der Pulsenergie Q zu 10 % der Pulsdauer (10 % Pulsbreite)
τ10, wie in Gleichung (2) gezeigt.
4 Produktzusammensetzung und grundlegende Parameter
4.1 Zusammensetzung des Behandlungsinstruments
a) Kohlendioxidlaser;
b) Energie- und Steuerungssysteme;
c) Sicherheitsschutzsystem;
d) Ziel- und Übertragungssysteme;
e) Kühlsysteme;
f) Ausgabesysteme und Zubehör (darunter ggf. Ausgabehandwerkzeuge,
Scangeräte/Matrix-Ausgabegeräte usw.).
4.2 Grundparameter des Behandlungsinstruments
a) Wellenlänge und Behandlungsart des Lasers;
b) Ausgangsimpulsenergie Q des Behandlungslaserterminals, Impulsfolgeenergie Qtrain,
Durchschnittsleistung Pav, Pulsleistung P50 und P10;
c) Behandlungslaserpulsdauer (Pulsbreite) τ (τ50 und τ10), Pulswiederholung
Periode T oder Pulswiederholfrequenz f oder Tastverhältnis η (siehe Abbildung 1 und
2);
d) Dauer des Behandlungslaserpulszugs (Pulszugbreite) T1, Pulszugzeit
Intervall T2 (siehe Abbildung 2) oder Pulsfolgewiederholungsperiode Ttrain; In-Train
Impulszahl n, Impulsdauer (Impulsbreite) τ (τ50 und τ10), die
Zugimpulswiederholungsperiode T (SIEHE Abbildung 1 und 2);
e) Divergenzwinkel am Ausgang des Behandlungslasers, Brennpunkt (Lichtpunkt)
Durchmesser;
f) Ziellichtwellenlänge;
g) Zielgerichtete Lichtleistung.
4.3 Sicherheitskategorie
Der Hersteller muss in der eingetragenen
Produktnormen.
a) Klasse und Typ gemäß den Bestimmungen von GB 9706.1;
b) Kategorie der Laserstrahlung gemäß GB 7247.1.
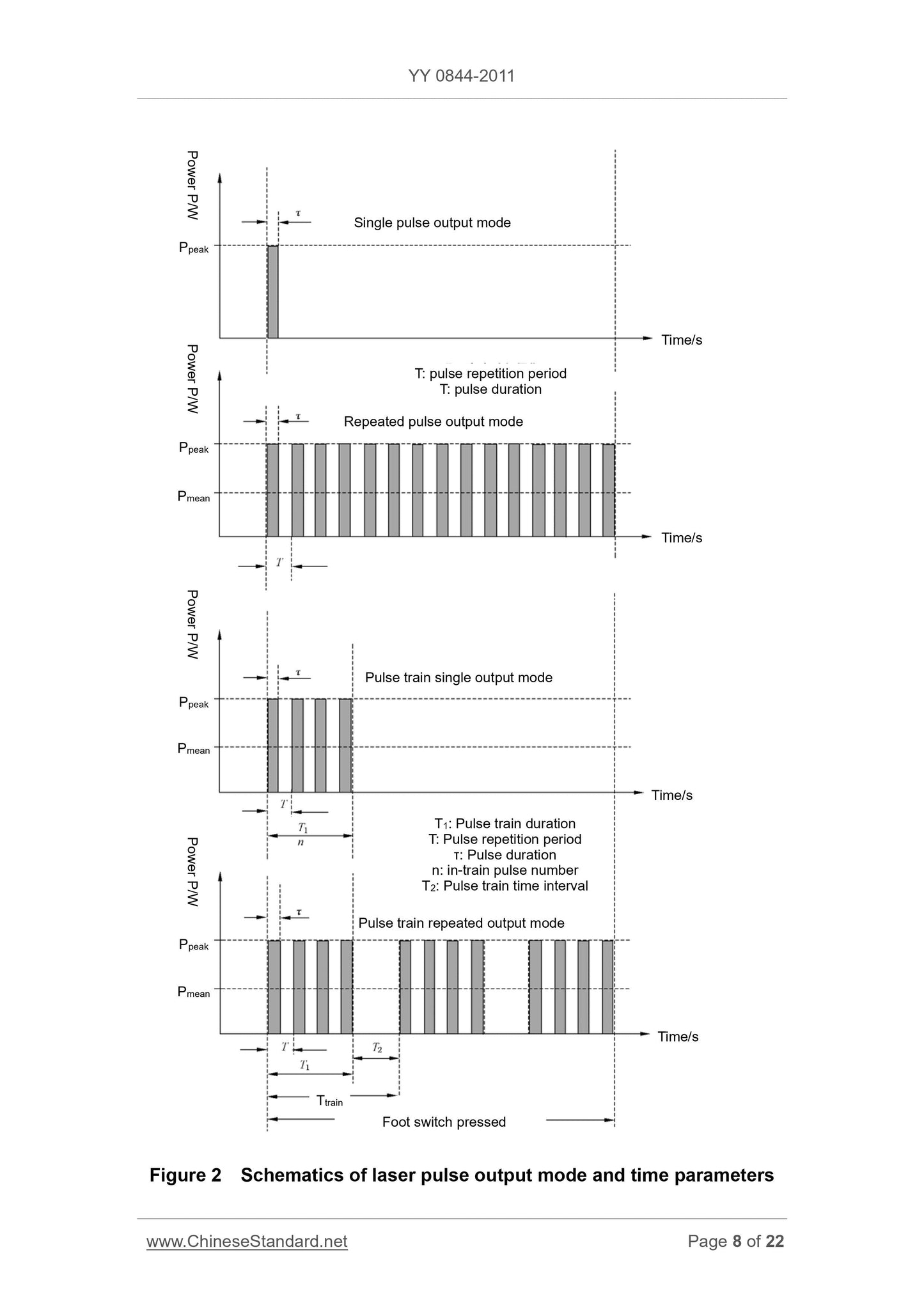
Abbildung 2 Schematische Darstellung des Laserpulsausgabemodus und der Zeitparameter
Einzelimpuls-Ausgabemodus
Leistung P/W
Spitze
Leistung P/W
Spitze
Leistung P/W
Pmean
Spitze
Pmean
Leistung P/W
Spitze
Pmean
Wiederholter Impulsausgabemodus
T. Pulswiederholperiode
T. Impulsdauer
Mal
Mal
Impulsfolge-Einzelausgangsmodus
Impulsfolge-Ausgabemodus mit wiederholter Ausgabe
Fußschalter gedrückt
Mal
Mal
T1. Dauer der Impulsfolge
T. Pulswiederholperiode
τ. Impulsdauer
n. In-Train-Pulszahl
T2. Impulsfolgezeitintervall
Zug
5 Anforderungen
5.1 Normale Betriebsbedingungen
Der Hersteller muss mindestens die folgenden Parameter für normale
Betriebsbedingungen.
- Umgebungstemperatur;
-...
Erhalten Sie in 1 Minute ein ANGEBOT: Klicken Sie auf YY 0844-2011
Historische Versionen: YY 0844-2011
Vorschau von True-PDF (Neu laden/Scrollen, wenn leer)
YY 0844-2011: Lasertherapiegerät. Behandlungsgerät mit gepulstem Kohlendioxidlaser
JJ 0844-2011
JJ
PHARMAZEUTISCHER INDUSTRIESTANDARD
DER VOLKSREPUBLIK CHINA
ICS 11.040.60
C 41
Lasertherapiegeräte –
Gepulstes Kohlendioxid-Laser-Behandlungsinstrument
激光治疗设备
AUSGESTELLT AM 31. DEZEMBER 2011
IMPLEMENTIERT AM 01. JUNI 2013
Herausgegeben von der chinesischen Arzneimittel- und Lebensmittelbehörde
Inhaltsverzeichnis
Vorwort ... 3
1 Geltungsbereich ... 4
2 Normative Verweisungen ... 4
3 Begriffe und Definitionen ... 5
4 Produktzusammensetzung und Grundparameter ... 6
5 Anforderungen ... 9
6 Prüfmethoden ... 14
7 Inspektionsregeln ... 19
8 Kennzeichnung, Etikett und Bedienungsanleitung ... 20
9 Verpackung, Transport und Lagerung ... 22
Vorwort
Dieser Standard wurde entsprechend den in GB/T 1.1.2009 festgelegten Regeln erstellt.
Diese Norm implementiert GB 9706.1-2007 „Medizinische elektrische Geräte - Teil
1. Allgemeine Anforderungen an die Sicherheit“, GB 9706.20-2000 „Medizinische elektrische
Geräte - Teil 2. Besondere Anforderungen an die Sicherheit von Diagnose- und
therapeutische Lasergeräte“ UND GB 7247.1-2001 „Sicherheit von Laserprodukten –
Teil 1. Geräteklassifizierung, Anforderungen und Benutzerhandbuch“.
Bitte beachten Sie, dass einige der Inhalte dieses Dokuments sich auf
Patente. Der Herausgeber dieses Dokuments ist nicht verantwortlich für die Identifizierung solcher
Patente.
Dieser Standard wurde von der China Food and Drug Administration vorgeschlagen.
Dieser Standard unterliegt der Zuständigkeit der National Medical Optics und
Technischer Ausschuss für Instrumentenstandardisierung (SAC/TC 103/SC 1).
Dieser Standard wurde von der China Food and Drug Administration Hangzhou erstellt
Zentrum für Qualitätsüberwachung und Inspektion von Medizinprodukten, Zhejiang Medical
Device Testing Institute und Chongqing Jingyu Laser Technology Co., Ltd.
Die Hauptverfasser dieser Norm. Han Jiancheng, Zhou Zhikang, Du Kun, Ye
Yueshun, Kong Peng.
Lasertherapiegeräte –
Gepulstes Kohlendioxid-Laser-Behandlungsinstrument
1 Geltungsbereich
Diese Norm legt die grundlegenden Parameter und die Zusammensetzung des Produkts fest.
technische Anforderungen, Prüfmethoden, Kennzeichnung Etiketten und Verpackung von gepulsten
Kohlendioxid-Laserbehandlungsgerät. Diese Norm bietet technische
Spezifikationen für Hersteller von gepulsten Kohlendioxid-Laserbehandlungen
Instrument zur Entwicklung von Produktnormen für Medizinprodukte.
Diese Norm gilt für den gepulsten Betriebsabschnitt der gepulsten Kohlenstoff
Kohlendioxid-Laserbehandlungsgerät mit nur gepulstem Betriebsmodus
UND das gepulste Kohlendioxid-Laser-Behandlungsinstrument, das sowohl die
Dauerwellenbetrieb und gepulster Betrieb (im Folgenden
einfach als Behandlungsinstrument bezeichnet) eines Kohlendioxidlasers
therapeutische Geräte, die sowohl a. Der Begriff „Puls“ in dieser Norm hat
die Pulsdauer (Pulsbreite) weniger als 0,25 s. Das Behandlungsinstrument ist,
über den Pulslaser mit einer Wellenlänge von 10,6 μm, der Verdampfung durchführt,
Karbonisierung, Koagulation und Bestrahlung des menschlichen Gewebes, um
den Behandlungszweck zu erreichen.
Was das gepulste Kohlendioxid-Laser-Behandlungsinstrument betrifft, das sowohl die
Dauerwellenbetrieb und gepulster Betrieb, der Dauerwellenbetrieb
Der Wellenbetrieb muss GB 11748 entsprechen, und der gepulste Betrieb
Der Modus muss diesem Standard entsprechen.
2 Normative Verweisungen
Die folgenden Dokumente sind für die Anwendung dieses Dokuments erforderlich.
die datierten Dokumente, es gelten nur die Versionen mit den angegebenen Daten
zu diesem Dokument; für die undatierten Dokumente gilt nur die neueste Version (einschließlich
alle Änderungen) sind auf diesen Standard anwendbar.
GB/T 191 Verpackung - Bildliche Kennzeichnung für den Umgang mit Waren
GB 7247.1 Sicherheit von Laserprodukten - Teil 1. Geräteklassifizierung,
Anforderungen und Benutzerhandbuch
GB 9706.1 Medizinische elektrische Geräte - Teil 1. Allgemeine Anforderungen an
Sicherheit
GB 9706.20 Medizinische elektrische Geräte - Teil 2. Besondere Anforderungen
für die Sicherheit diagnostischer und therapeutischer Lasergeräte
GB/T 14710 Umweltanforderungen und Prüfverfahren für medizinische
Elektrische Ausrüstung
GB/T 17736 Prüfverfahren für die wichtigsten Parameter von Laserschutzbrillen
YY 91057 Allgemeine Spezifikation für medizinische Fußschalter
ISO 11146 Laser und laserbezogene Einrichtungen - Prüfverfahren für Laserstrahlen
Breiten, Divergenzwinkel und Strahlausbreitungsverhältnisse
3 Begriffe und Definitionen
Die Begriffe und Definitionen wie in GB 7247.1 definiert UND die folgenden gelten für
dieses Dokument.
3.1
50%-Pulsdauer
τ50
Es bezeichnet die Zeitspanne zwischen dem Anstieg und Abfall des Laserpulses bis zu seiner
50 % Spitzenleistungspunkt, wie in Abbildung 1 dargestellt.
Abbildung 1 Schematische Darstellung der Laserpulsdauer (Pulsbreite) und
Pulswiederholperiode
3.2
Zeit
Leistung
P-Spitze
50 % P
10 % P
Pulswiederholperiode (T)
10%-Pulsdauer
τ10
Es bezeichnet die Zeitspanne zwischen dem Anstieg und Abfall des Laserpulses bis zu seiner
10 % Spitzenleistungspunkt, wie in Abbildung 1 dargestellt.
3.3
50%-Pulsleistung
P50
P50 ist das Verhältnis von Pulsenergie Q zu 50%-Pulsdauer (50% Pulsbreite)
τ50, wie in Gleichung (1) gezeigt.
3.4
10%-Pulsleistung
Platz 10
P10 ist das Verhältnis der Pulsenergie Q zu 10 % der Pulsdauer (10 % Pulsbreite)
τ10, wie in Gleichung (2) gezeigt.
4 Produktzusammensetzung und grundlegende Parameter
4.1 Zusammensetzung des Behandlungsinstruments
a) Kohlendioxidlaser;
b) Energie- und Steuerungssysteme;
c) Sicherheitsschutzsystem;
d) Ziel- und Übertragungssysteme;
e) Kühlsysteme;
f) Ausgabesysteme und Zubehör (darunter ggf. Ausgabehandwerkzeuge,
Scangeräte/Matrix-Ausgabegeräte usw.).
4.2 Grundparameter des Behandlungsinstruments
a) Wellenlänge und Behandlungsart des Lasers;
b) Ausgangsimpulsenergie Q des Behandlungslaserterminals, Impulsfolgeenergie Qtrain,
Durchschnittsleistung Pav, Pulsleistung P50 und P10;
c) Behandlungslaserpulsdauer (Pulsbreite) τ (τ50 und τ10), Pulswiederholung
Periode T oder Pulswiederholfrequenz f oder Tastverhältnis η (siehe Abbildung 1 und
2);
d) Dauer des Behandlungslaserpulszugs (Pulszugbreite) T1, Pulszugzeit
Intervall T2 (siehe Abbildung 2) oder Pulsfolgewiederholungsperiode Ttrain; In-Train
Impulszahl n, Impulsdauer (Impulsbreite) τ (τ50 und τ10), die
Zugimpulswiederholungsperiode T (SIEHE Abbildung 1 und 2);
e) Divergenzwinkel am Ausgang des Behandlungslasers, Brennpunkt (Lichtpunkt)
Durchmesser;
f) Ziellichtwellenlänge;
g) Zielgerichtete Lichtleistung.
4.3 Sicherheitskategorie
Der Hersteller muss in der eingetragenen
Produktnormen.
a) Klasse und Typ gemäß den Bestimmungen von GB 9706.1;
b) Kategorie der Laserstrahlung gemäß GB 7247.1.
Abbildung 2 Schematische Darstellung des Laserpulsausgabemodus und der Zeitparameter
Einzelimpuls-Ausgabemodus
Leistung P/W
Spitze
Leistung P/W
Spitze
Leistung P/W
Pmean
Spitze
Pmean
Leistung P/W
Spitze
Pmean
Wiederholter Impulsausgabemodus
T. Pulswiederholperiode
T. Impulsdauer
Mal
Mal
Impulsfolge-Einzelausgangsmodus
Impulsfolge-Ausgabemodus mit wiederholter Ausgabe
Fußschalter gedrückt
Mal
Mal
T1. Dauer der Impulsfolge
T. Pulswiederholperiode
τ. Impulsdauer
n. In-Train-Pulszahl
T2. Impulsfolgezeitintervall
Zug
5 Anforderungen
5.1 Normale Betriebsbedingungen
Der Hersteller muss mindestens die folgenden Parameter für normale
Betriebsbedingungen.
- Umgebungstemperatur;
-...
Aktie