1
/
von
12
PayPal, credit cards. Download editable-PDF & invoice in 1 second!
YY/T 1095-2015 Englisch PDF (YYT1095-2015)
YY/T 1095-2015 Englisch PDF (YYT1095-2015)
Normaler Preis
$165.00 USD
Normaler Preis
Verkaufspreis
$165.00 USD
Grundpreis
/
pro
Versand wird beim Checkout berechnet
Verfügbarkeit für Abholungen konnte nicht geladen werden
Lieferung: 3 Sekunden. True-PDF + Rechnung herunterladen.
Erhalten Sie in 1 Minute ein ANGEBOT: Klicken Sie auf YY/T 1095-2015
Historische Versionen: YY/T 1095-2015
Vorschau von True-PDF (Neu laden/Scrollen, wenn leer)
YY/T 1095-2015: Myoelektrisches Biofeedback-Gerät
JJ/T 1095-2015
JJ
PHARMAINDUSTRIE-STANDARD
DER VOLKSREPUBLIK CHINA
ICS 11.040.60
C 42
Ersetzt YY/T 1095-2007
Myoelektrische Biofeedback-Ausrüstung
AUSGESTELLT AM 2. MÄRZ 2015
IMPLEMENTIERT AM 1. JANUAR 2016
Herausgegeben von der chinesischen Lebensmittel- und Arzneimittelbehörde
Inhaltsverzeichnis
Vorwort ... 3
1 Geltungsbereich ... 5
2 Normative Verweisungen ... 5
3 Begriffe und Definitionen ... 5
4 Klassifizierung ... 6
5 Anforderungen ... 6
6 Testmethoden ... 10
Anhang A (Informativ) Leitlinie und Grundsatz wichtiger Klauseln ... 16
Literaturverzeichnis ... 21
Vorwort
Dieser Standard wurde gemäß den in GB/T 1.1-2009 festgelegten Regeln erstellt.
Die Sicherheitsanforderungen dieser Norm setzen die Inhalte von GB 9706.1-2007 vollständig um.
Medizinische elektrische Geräte - Teil 1. Allgemeine Anforderungen an die Sicherheit und GB
9706.15-2008 Medizinische elektrische Geräte - Teil 1-1. Allgemeine Anforderungen für
Sicherheit - Ergänzungsnorm. Sicherheitsanforderungen für medizinische elektrische Systeme.
Diese Norm ersetzt YY/T 1095-2007 Myoelektrische Biofeedback-Ausrüstung.
Im Vergleich zu YY/T 1095-2007 weist dieser Standard im Wesentlichen folgende technische
Unterschiede.
--- Den Anwendungsbereich dieser Norm ändern (siehe Kapitel 1);
--- Fügen Sie die Klassifizierung hinzu (siehe Kapitel 4);
--- Modifizierung der Anforderungen an Feedback-Anweisungen und Testmethoden (siehe 5.2, 6.2
dieser Ausgabe; 4.2.7, 5.2 der Ausgabe 2007);
--- Anforderungen an Rückkopplungsschwellenwerte und Testmethoden hinzufügen (siehe 5.3, 6.3);
--- Anforderungen an die Unterdrückung von Netzfrequenzrauschen hinzufügen und testen
Methoden (siehe 5.4, 6.3);
--- Streichung der Anforderungen an den ursprünglichen Messbereich und die Prüfmethoden (siehe
4.2.1, 5.3.1 der Ausgabe 2007);
--- Anforderungen an die Genauigkeit der Anzeigewerte und Prüfverfahren hinzufügen (siehe
5.5.2, 6.5.1);
--- Streichung der Anforderungen an die ursprüngliche Sensibilität (siehe 4.2.8 der Ausgabe 2007);
--- Anforderungen an Auflösung und Prüfverfahren hinzufügen (siehe 5.5.3, 6.5.2);
--- Ändern Sie die Anforderungen an Durchlassband und Testmethoden (siehe 5.5.5, 6.5.4 dieser
Ausgabe; und 4.2.4, 5.3.4 der Ausgabe 2007);
--- Anforderungen an Netzfrequenz-Sperrfilter und Prüfverfahren hinzufügen (siehe
5.5.8, 6.5.7);
--- Die Anforderungen an die ursprüngliche Isolierung werden gelöscht (siehe 4.2.9 der Ausgabe 2007).
--- Sicherheitsanforderungen hinzufügen (siehe 5.8);
--- Inhalte und Anforderungen für die Bedienungsanleitung hinzufügen (siehe 5.7);
Myoelektrische Biofeedback-Ausrüstung
1 Geltungsbereich
Diese Norm legt die Begriffe, Klassifizierung, Anforderungen, Prüf- und
Methoden der myoelektrischen Biofeedback-Geräte (im Folgenden als
myoelektrische Biofeedback-Geräte).
Diese Norm ist auf die in 3.1 genannte myoelektrische Biofeedback-Ausrüstung anwendbar.
Diese Norm gilt nicht für Geräte mit Nadelelektroden zur Aufzeichnung der
myoelektrisches Signal und myoelektrisch evozierte Potenzialausrüstung.
2 Normative Verweisungen
Die folgenden Dokumente sind für die Anwendung dieses Dokuments erforderlich. Für die
datierte Dokumente, sind für diese nur die Versionen mit den angegebenen Daten gültig
Dokument; bei undatierten Dokumenten wird nur die neueste Version (einschließlich aller
Änderungen) sind auf dieses Dokument anwendbar.
GB 9706.1-2007 Medizinische elektrische Geräte - Teil 1. Allgemeine Anforderungen für
Sicherheit
GB 9706.15-2008 Medizinische elektrische Geräte - Teil 1-1. Allgemeine Anforderungen
für Sicherheit - Ergänzungsnorm. Sicherheitsanforderungen für medizinische elektrische
Systeme
GB/T 14710-2009 Umweltanforderungen und Testmethoden für medizinische
Elektrische Ausrüstung
GB/T 16886.1-2011 Biologische Bewertung von Medizinprodukten - Teil 1. Bewertung
und Testen im Rahmen eines Risikomanagementprozesses
YY 0505-2012 Medizinische elektrische Geräte - Teil 1-2. Allgemeine Anforderungen für
Sicherheit - Ergänzende Normen. Elektromagnetische Verträglichkeit - Anforderungen und
Tests
3 Begriffe und Definitionen
Die folgenden in GB 9706.1-2007 definierten Begriffe und Definitionen sind auf diese anwendbar
5.6.1 Die Oberfläche des myoelektrischen Biofeedback-Gerätes muss glatt sein, seine Markierung muss
klar und präzise sein, ohne sichtbare Kratzer oder Beschädigungen.
5.6.2 Die Befestigungselemente müssen fest verbunden sein, der Funktionsschalter muss sorgfältig installiert werden.
Die Einstellung muss zuverlässig sein.
5.7 Bedienungsanleitung
Die Bedienungsanleitung muss den Anforderungen der GB 9706.1-2007 und GB entsprechen.
9706.15-2008 (falls zutreffend); in der Zwischenzeit muss es auch mindestens Folgendes enthalten
Inhalt.
a) Zu den technischen Parametern der myoelektrischen Biofeedback-Geräte gehören
Messbereich der Amplitude, Rückkopplungsfrequenzband, Mitte
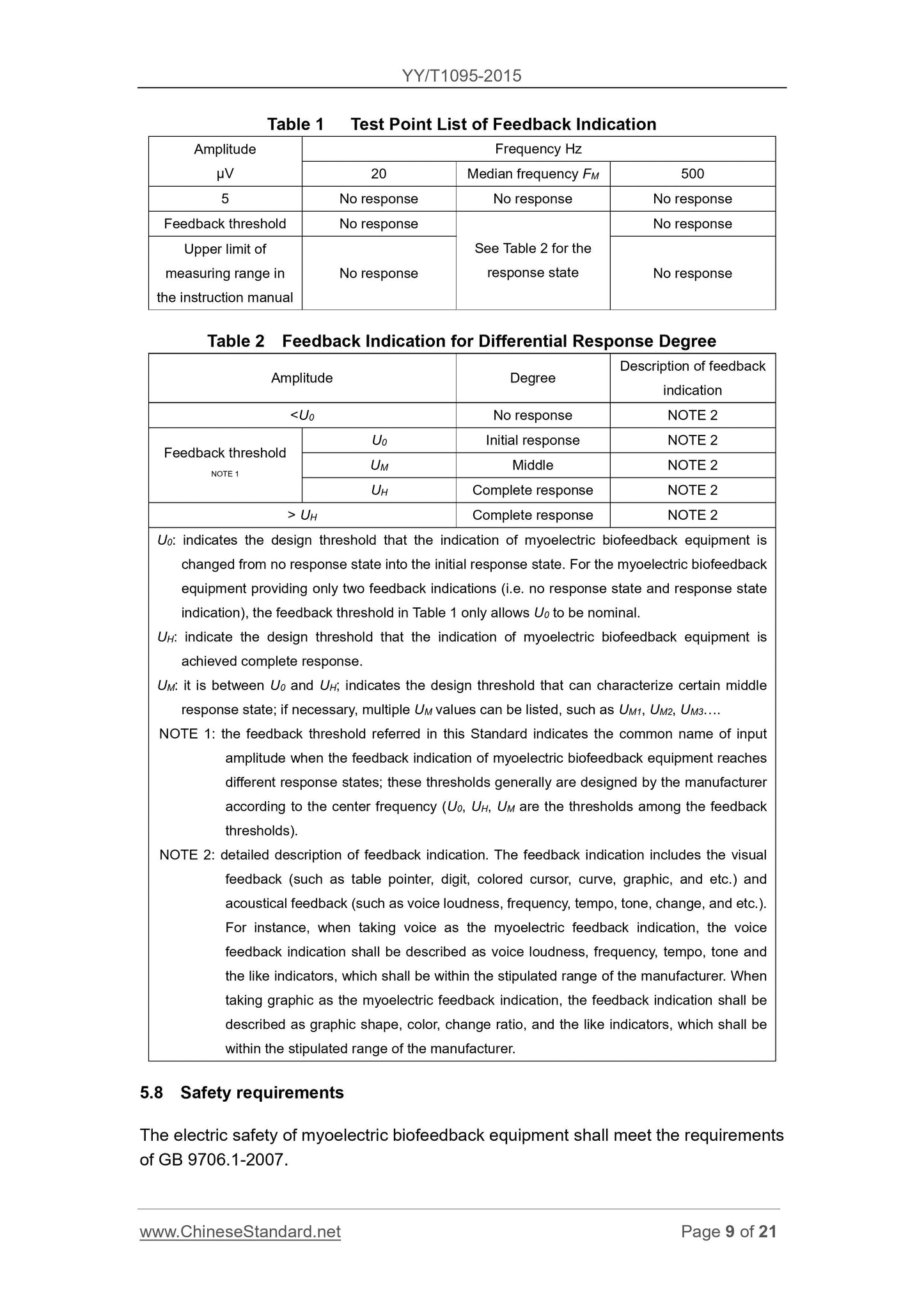
Frequenz und die in Tabelle 1 festgelegten Prüfpunkte.
b) Reinigungs- und Desinfektionsmethoden sowie Austauschzyklus für die wiederverwendbaren
Elektrode.
c) Geben Sie eine Methode an, mit der die Elektrode festen Kontakt mit der Haut hat;
wie man die Haut vor der Behandlung behandelt.
d) Die Beziehung zwischen Elektrodengröße, Form und betroffenem Muskel; die
Hinweise zur Position und Entfernung der Elektrodenplatzierung.
e) Empfohlene Einsatzumgebung. Die Quelle hochfrequenter Störungen darf
ausgeschaltet sein oder sich von der Hochfrequenz-Emissionsquelle fernhalten.
f) In der Bedienungsanleitung die Feedback-Anzeige des myoelektrischen Biofeedbacks
Die Ausrüstung wird gemäß den verschiedenen Rückkopplungsreaktionsgraden beschrieben
sind in Tabelle 2 festgelegt.
Für das myoelektrische Biofeedback-Gerät mit nur zwei Feedback-Reaktionen,
die Bedienungsanleitung muss entsprechende Rückmeldungen enthalten
Beschreibung gegenüber den beiden Feedback-Antworten, nämlich keine Antwort und
erste Antwort.
Sofern vom Hersteller nicht anders angegeben, muss das Eingangssignal
nach den in Tabelle 1 angegebenen Prüfpunkten geprüft werden; ggf.
Diese Testpunkte können erweitert werden, so dass sie andere charakteristische
Die vom Hersteller festgelegten Parameterwerte.
Gegebenenfalls muss die elektrische Sicherheit des Systems den Anforderungen der GB entsprechen.
9706.15-2008.
5.9 Anforderungen an Umweltprüfungen
Der Umwelttest der myoelektrischen Biofeedback-Ausrüstung muss durchgeführt werden
gemäß den Bestimmungen von GB/T 14710-2009.
5.10 Biokompatibilität
Materialien, die für den Kontakt mit der menschlichen Haut vorgesehen sind, müssen
Biokompatibilitätstest oder -bewertung und Formulardokument gemäß Leitlinie und
Grundsatz festgelegt in GB/T 16886.1-2011.
5.11 Anforderungen an die elektromagnetische Verträglichkeit
Myoelektrische Biofeedback-Geräte müssen die Anforderungen von YY 0505-2012 erfüllen.
6 Testmethoden
6.1 Arbeitsbedingungen
6.1.1 Vorbehandlung
Vor dem Test muss das myoelektrische Biofeedback-Gerät auf dem Testgelände abgestellt werden,
mindestens 24 Stunden ohne Energiezufuhr; vor dem offiziellen Test wird die myoelektrische
Biofeedback-Geräte müssen entsprechend den Anforderungen der Bedienungsanleitung betrieben werden.
6.1.2 Testumgebung
Siehe die Anforderung 4.5 in GB 9706.1-2007.
Schalten Sie die umgebende Hochfrequenzstörquelle aus oder halten Sie sich davon fern.
6.1.3 Prüfschaltung
Die Anschlussmethode des Prüfkreises soll wie folgt dargestellt werden.
a) Sofern nicht anders angegeben, muss S1 in Abbildung 1 normalerweise geschlossen sein.
b) Die Referenzelektrode (sofern vorhanden) muss geerdet sein.
c) Die gestrichelte Linie in Abbildung 1 stellt das Abschirmgehäuse und den Referenzpunkt dar
Verbindung zur Erde herstellen.
entsprechend der in Tabelle 1 beschriebenen Rückkopplungsschwelle, zeichnen Sie das Signal auf
Amplitude zu diesem Zeitpunkt, und vergleichen Sie diese mit der Rückkopplungsschwelle, die durch
der Hersteller; der Fehler muss den Bestimmungen von 5.3 entsprechen.
6.4 Überprüfung der Kraftfahr...
Erhalten Sie in 1 Minute ein ANGEBOT: Klicken Sie auf YY/T 1095-2015
Historische Versionen: YY/T 1095-2015
Vorschau von True-PDF (Neu laden/Scrollen, wenn leer)
YY/T 1095-2015: Myoelektrisches Biofeedback-Gerät
JJ/T 1095-2015
JJ
PHARMAINDUSTRIE-STANDARD
DER VOLKSREPUBLIK CHINA
ICS 11.040.60
C 42
Ersetzt YY/T 1095-2007
Myoelektrische Biofeedback-Ausrüstung
AUSGESTELLT AM 2. MÄRZ 2015
IMPLEMENTIERT AM 1. JANUAR 2016
Herausgegeben von der chinesischen Lebensmittel- und Arzneimittelbehörde
Inhaltsverzeichnis
Vorwort ... 3
1 Geltungsbereich ... 5
2 Normative Verweisungen ... 5
3 Begriffe und Definitionen ... 5
4 Klassifizierung ... 6
5 Anforderungen ... 6
6 Testmethoden ... 10
Anhang A (Informativ) Leitlinie und Grundsatz wichtiger Klauseln ... 16
Literaturverzeichnis ... 21
Vorwort
Dieser Standard wurde gemäß den in GB/T 1.1-2009 festgelegten Regeln erstellt.
Die Sicherheitsanforderungen dieser Norm setzen die Inhalte von GB 9706.1-2007 vollständig um.
Medizinische elektrische Geräte - Teil 1. Allgemeine Anforderungen an die Sicherheit und GB
9706.15-2008 Medizinische elektrische Geräte - Teil 1-1. Allgemeine Anforderungen für
Sicherheit - Ergänzungsnorm. Sicherheitsanforderungen für medizinische elektrische Systeme.
Diese Norm ersetzt YY/T 1095-2007 Myoelektrische Biofeedback-Ausrüstung.
Im Vergleich zu YY/T 1095-2007 weist dieser Standard im Wesentlichen folgende technische
Unterschiede.
--- Den Anwendungsbereich dieser Norm ändern (siehe Kapitel 1);
--- Fügen Sie die Klassifizierung hinzu (siehe Kapitel 4);
--- Modifizierung der Anforderungen an Feedback-Anweisungen und Testmethoden (siehe 5.2, 6.2
dieser Ausgabe; 4.2.7, 5.2 der Ausgabe 2007);
--- Anforderungen an Rückkopplungsschwellenwerte und Testmethoden hinzufügen (siehe 5.3, 6.3);
--- Anforderungen an die Unterdrückung von Netzfrequenzrauschen hinzufügen und testen
Methoden (siehe 5.4, 6.3);
--- Streichung der Anforderungen an den ursprünglichen Messbereich und die Prüfmethoden (siehe
4.2.1, 5.3.1 der Ausgabe 2007);
--- Anforderungen an die Genauigkeit der Anzeigewerte und Prüfverfahren hinzufügen (siehe
5.5.2, 6.5.1);
--- Streichung der Anforderungen an die ursprüngliche Sensibilität (siehe 4.2.8 der Ausgabe 2007);
--- Anforderungen an Auflösung und Prüfverfahren hinzufügen (siehe 5.5.3, 6.5.2);
--- Ändern Sie die Anforderungen an Durchlassband und Testmethoden (siehe 5.5.5, 6.5.4 dieser
Ausgabe; und 4.2.4, 5.3.4 der Ausgabe 2007);
--- Anforderungen an Netzfrequenz-Sperrfilter und Prüfverfahren hinzufügen (siehe
5.5.8, 6.5.7);
--- Die Anforderungen an die ursprüngliche Isolierung werden gelöscht (siehe 4.2.9 der Ausgabe 2007).
--- Sicherheitsanforderungen hinzufügen (siehe 5.8);
--- Inhalte und Anforderungen für die Bedienungsanleitung hinzufügen (siehe 5.7);
Myoelektrische Biofeedback-Ausrüstung
1 Geltungsbereich
Diese Norm legt die Begriffe, Klassifizierung, Anforderungen, Prüf- und
Methoden der myoelektrischen Biofeedback-Geräte (im Folgenden als
myoelektrische Biofeedback-Geräte).
Diese Norm ist auf die in 3.1 genannte myoelektrische Biofeedback-Ausrüstung anwendbar.
Diese Norm gilt nicht für Geräte mit Nadelelektroden zur Aufzeichnung der
myoelektrisches Signal und myoelektrisch evozierte Potenzialausrüstung.
2 Normative Verweisungen
Die folgenden Dokumente sind für die Anwendung dieses Dokuments erforderlich. Für die
datierte Dokumente, sind für diese nur die Versionen mit den angegebenen Daten gültig
Dokument; bei undatierten Dokumenten wird nur die neueste Version (einschließlich aller
Änderungen) sind auf dieses Dokument anwendbar.
GB 9706.1-2007 Medizinische elektrische Geräte - Teil 1. Allgemeine Anforderungen für
Sicherheit
GB 9706.15-2008 Medizinische elektrische Geräte - Teil 1-1. Allgemeine Anforderungen
für Sicherheit - Ergänzungsnorm. Sicherheitsanforderungen für medizinische elektrische
Systeme
GB/T 14710-2009 Umweltanforderungen und Testmethoden für medizinische
Elektrische Ausrüstung
GB/T 16886.1-2011 Biologische Bewertung von Medizinprodukten - Teil 1. Bewertung
und Testen im Rahmen eines Risikomanagementprozesses
YY 0505-2012 Medizinische elektrische Geräte - Teil 1-2. Allgemeine Anforderungen für
Sicherheit - Ergänzende Normen. Elektromagnetische Verträglichkeit - Anforderungen und
Tests
3 Begriffe und Definitionen
Die folgenden in GB 9706.1-2007 definierten Begriffe und Definitionen sind auf diese anwendbar
5.6.1 Die Oberfläche des myoelektrischen Biofeedback-Gerätes muss glatt sein, seine Markierung muss
klar und präzise sein, ohne sichtbare Kratzer oder Beschädigungen.
5.6.2 Die Befestigungselemente müssen fest verbunden sein, der Funktionsschalter muss sorgfältig installiert werden.
Die Einstellung muss zuverlässig sein.
5.7 Bedienungsanleitung
Die Bedienungsanleitung muss den Anforderungen der GB 9706.1-2007 und GB entsprechen.
9706.15-2008 (falls zutreffend); in der Zwischenzeit muss es auch mindestens Folgendes enthalten
Inhalt.
a) Zu den technischen Parametern der myoelektrischen Biofeedback-Geräte gehören
Messbereich der Amplitude, Rückkopplungsfrequenzband, Mitte
Frequenz und die in Tabelle 1 festgelegten Prüfpunkte.
b) Reinigungs- und Desinfektionsmethoden sowie Austauschzyklus für die wiederverwendbaren
Elektrode.
c) Geben Sie eine Methode an, mit der die Elektrode festen Kontakt mit der Haut hat;
wie man die Haut vor der Behandlung behandelt.
d) Die Beziehung zwischen Elektrodengröße, Form und betroffenem Muskel; die
Hinweise zur Position und Entfernung der Elektrodenplatzierung.
e) Empfohlene Einsatzumgebung. Die Quelle hochfrequenter Störungen darf
ausgeschaltet sein oder sich von der Hochfrequenz-Emissionsquelle fernhalten.
f) In der Bedienungsanleitung die Feedback-Anzeige des myoelektrischen Biofeedbacks
Die Ausrüstung wird gemäß den verschiedenen Rückkopplungsreaktionsgraden beschrieben
sind in Tabelle 2 festgelegt.
Für das myoelektrische Biofeedback-Gerät mit nur zwei Feedback-Reaktionen,
die Bedienungsanleitung muss entsprechende Rückmeldungen enthalten
Beschreibung gegenüber den beiden Feedback-Antworten, nämlich keine Antwort und
erste Antwort.
Sofern vom Hersteller nicht anders angegeben, muss das Eingangssignal
nach den in Tabelle 1 angegebenen Prüfpunkten geprüft werden; ggf.
Diese Testpunkte können erweitert werden, so dass sie andere charakteristische
Die vom Hersteller festgelegten Parameterwerte.
Gegebenenfalls muss die elektrische Sicherheit des Systems den Anforderungen der GB entsprechen.
9706.15-2008.
5.9 Anforderungen an Umweltprüfungen
Der Umwelttest der myoelektrischen Biofeedback-Ausrüstung muss durchgeführt werden
gemäß den Bestimmungen von GB/T 14710-2009.
5.10 Biokompatibilität
Materialien, die für den Kontakt mit der menschlichen Haut vorgesehen sind, müssen
Biokompatibilitätstest oder -bewertung und Formulardokument gemäß Leitlinie und
Grundsatz festgelegt in GB/T 16886.1-2011.
5.11 Anforderungen an die elektromagnetische Verträglichkeit
Myoelektrische Biofeedback-Geräte müssen die Anforderungen von YY 0505-2012 erfüllen.
6 Testmethoden
6.1 Arbeitsbedingungen
6.1.1 Vorbehandlung
Vor dem Test muss das myoelektrische Biofeedback-Gerät auf dem Testgelände abgestellt werden,
mindestens 24 Stunden ohne Energiezufuhr; vor dem offiziellen Test wird die myoelektrische
Biofeedback-Geräte müssen entsprechend den Anforderungen der Bedienungsanleitung betrieben werden.
6.1.2 Testumgebung
Siehe die Anforderung 4.5 in GB 9706.1-2007.
Schalten Sie die umgebende Hochfrequenzstörquelle aus oder halten Sie sich davon fern.
6.1.3 Prüfschaltung
Die Anschlussmethode des Prüfkreises soll wie folgt dargestellt werden.
a) Sofern nicht anders angegeben, muss S1 in Abbildung 1 normalerweise geschlossen sein.
b) Die Referenzelektrode (sofern vorhanden) muss geerdet sein.
c) Die gestrichelte Linie in Abbildung 1 stellt das Abschirmgehäuse und den Referenzpunkt dar
Verbindung zur Erde herstellen.
entsprechend der in Tabelle 1 beschriebenen Rückkopplungsschwelle, zeichnen Sie das Signal auf
Amplitude zu diesem Zeitpunkt, und vergleichen Sie diese mit der Rückkopplungsschwelle, die durch
der Hersteller; der Fehler muss den Bestimmungen von 5.3 entsprechen.
6.4 Überprüfung der Kraftfahr...
Aktie